Метаболизм одноуглеродных фрагментов. Роль фолиевой кислоты. Гипегомоцистеинемия.
3. Метилентетрагидрофолатредуктаза
МТНFR (метилен) – внутриклеточный фермент, участвующий в превращении гомоцистеина в метионин в присутствии кофакторов – пиридоксина (витамина В6) и цианокобаламина (витамина В12) – и субстрата – фолиевой кислоты. Активность фермента может снижаться в результате нуклеотидных замен в кодирующем его гене. Вследствие этого нарушается метаболический путь превращения гомоцистеина и его содержание в плазме крови увеличивается.
Метилентетрагидрофолатредуктаза (MTHFR) является ферментом, ограничивающим скорость, в метильном цикле и кодируется геном MTHFR. Метилентетрагидрофолатредуктаза катализирует превращение 5,10-метилентетрагидрофолата в 5-метилтетрагидрофолат, вещество для ремилирования гомоцистеина в метионин. Естественная вариабельность этого гена распространена у здоровых людей. Хотя сообщалось, что некоторые варианты влияют на восприимчивость к окклюзионным сосудистым заболеваниям, дефектам нервной трубки, болезни Альцгеймера и другим формам деменции, рака толстой кишки и острой лейкемии, результаты небольших ранних исследований не были воспроизведены. Некоторые мутации в этом гене связаны с дефицитом метилентетрагидрофолатредуктазы.
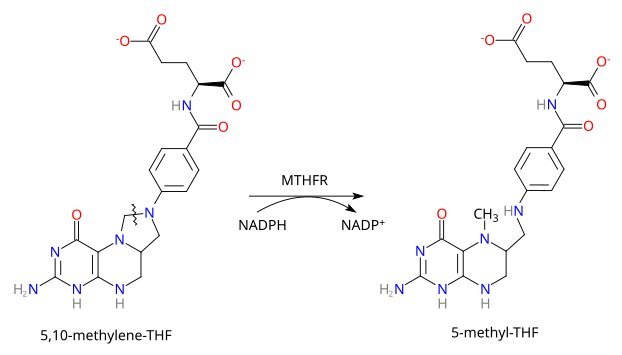
В метиловом цикле MTHFR необратимо восстанавливает 5,10-метилентетрагидрофолат (субстрат) до 5-метилтетрагидрофолата (продукт).
5,10-метилентетрагидрофолат используется для превращения dUMP в dTMP для синтеза de novo тимидина.
5-Метилтетрагидрофолат используется для превращения гомоцистеина (потенциально токсичной аминокислоты) в метионин ферментом метионин-синтазой. (Обратите внимание, что гомоцистеин также может быть превращен в метионин не зависящим от фолата ферментом бетаин-гомоцистеин метилтрансферазой (BHMT)). MTHFR содержит связанный флавин-кофактор и использует NAD (P) H в качестве восстановителя.
Активность MTHFR может ингибироваться связыванием дигидрофолата (DHF) и S-аденозилметионина (SAM или AdoMet). MTHFR также может быть фосфорилирован - это уменьшает его активность на ~ 20% и облегчает его ингибирование SAMом.
Среди всех известных генетических причин гипергомоцистеинемии наиболее распространены замены в гене MTHFR. Известно около десяти вариантов этого гена, влияющих на изменение функции кодируемого им фермента.
Самым изученным является вариант, в котором цитозин (С) в позиции 677 заменен на тимин (T). Такой полиморфизм MTHFR обозначается как C677Т SNP (Ala222Val) и сопровождается повышением уровня гомоцистеина в крови.
Другим вариантом полиморфизма гена MTHFR является замена нуклеотида аденина (A) на цитозин (С) в позиции 1298, приводящая к изменению структуры фермента, в котором глутаминовая кислота в позиции 429 меняется на аланин. Данная замена приводит к снижению активности фермента, более выраженному у носителей двух аллелей 1298С (генотип С/С). Биохимические характеристики измененного фермента не отличаются от свойств фермента дикого типа (неизмененного).
Комбинация генотипов 677 С/T и 1298 А/C сопровождается не только снижением активности фермента, но и повышением концентрации гомоцистеина в плазме и снижением уровня фолата, как это бывает при носительстве двух аллелей 677T. Кроме того, эта комбинация увеличивает вероятность дефектов нервной трубки у плода. Дефицит MTHFR способствует тератогенному (повреждающему плод) и мутагенному (повреждающему ДНК) действию из-за нарушения процессов метилирования ДНК.
Увеличение концентрации гомоцистеина повышает риск атеросклероза и тромбоза. Накапливаясь в организме, гомоцистеин повреждает внутреннюю стенку артерий, что приводит к разрывам эндотелия. На поврежденную поверхность осаждаются холестерин и кальций, образуя атеросклеротическую бляшку, вследствие чего просвет сосуда сужается, а иногда закупоривается.
В исследованиях был подтвержден протективный эффект присутствия аллеля 1298С при врожденных пороках сердца. Поскольку фермент MTHFR участвует в процессе синтеза нейромедиаторов (серотонина, мелатонина, дофамина, адреналина и др.), изменения функции белка могут влиять на умственную, эмоциональную и физическую деятельность.
Таким образом, присутствие аллеля С по маркеру А1298С может способствовать развитию в основном сердечно-сосудистых заболеваний и осложнений беременности, особенно в комбинации с нарушениями в работе других ферментов, а также в условиях наличия дополнительных факторов риска развития гипергомоцистеинемии или дефицита фолатов (нерациональное питание, лекарственная терапия, сопутствующие заболевания, вредные привычки).