Молекулярные мишени гиполипидемических средств
4. Антисмысловые олигонуклеотиды
Антисмысловые олигонуклеотиды (АСО) представляют собой синтетические одноцепочечные молекулы дезоксирибонуклеиновой кислоты (ДНК) длиной от 8 до 50 нуклеотидов, которые целиком или частично связываются с рибонуклеиновой кислотой (РНК) и препятствуют дальнейшей трансляции мРНК в белок (11). Подавление биосинтеза белка под действием АСО происходит вследствие того, что мРНК-мишень в составе гибридного ДНК/РНК комплекса с АСО расщепляется внутриклеточной РНКазой Н (12) (рис. 2).
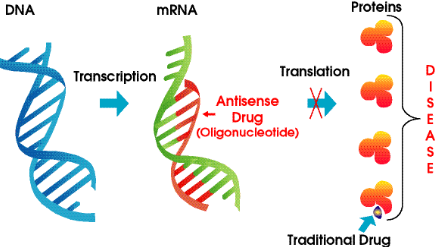
Впервые возможность избирательного подавления продукции определенного белка под действием АСО была продемонстрирована еще в 1978 г. в работе Р. Zamecnik и М. Stephenson (13). Авторы показали, что 13-звенный олигонуклеотид, комплементарный 3′-концевой последовательности РНК вируса саркомы Рауса, ингибирует репликацию вируса in vitro. Эта работа послужила толчком к изучению потенциала АСО в качестве ЛС для лечения вирусных заболеваний, воспалительных процессов, болезней крови, нарушений сердечно-сосудистой системы (14-18).
Ввиду того что природные олигодезоксирибонуклеотиды in vivo подвергаются быстрой деградации под действием нуклеаз, для повышения их стабильности в структуру АСО вносят различные химические модификации (19). Внесение модификаций в структуру олигонуклеотида не только повышает устойчивость АСО к нуклеазам, но и увеличивает эффективность их биологического действия, улучшает гибридизационные свойства и облегчает их захват клетками.
В первом поколении устойчивость к нуклеазам обеспечивалась модификацией фосфодиэфирной связи – замещение кислорода серой (фосфотиоаты), что позволяло повысить устойчивость препаратов к эндонуклеазам, не ухудшая при этом субстратные свойства комплекса относительно нуклеазы Н, однако затруднялось связывание АСО с целевой мРНК. Такие препараты АСО плохо проникали в клетку и имели ограниченный спектр распределения в органах и тканях. Препараты второго поколения были модифицированы по 2′-положению рибозы путем введения 2′-О-метильной, 2′-О-метоксиэтильной группы. Такая модификация позволяла повысить устойчивость к эндонуклеазам и снизить токсичность препарата, но ухудшала субстратные свойства дуплекса с целевой мРНК относительно РНКазы Н. Комбинация двух модификаций позволила получить АСО, обладающие хорошей специфичностью, селективностью и аффинностью к целевой молекуле (20). Химерные АСО, использующие одновременно фосфотиоатные и 2′-О-метоксиэтил или 2′-О-метил-модификации, легли в основу ЛС под названием «мипомерсен».